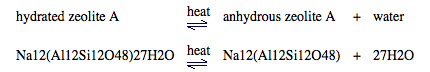Usos de la Zeolita para la destrucción del Ozono
La zeolita se usa comúnmente para la destrucción del ozono, ya que funciona para acelerar el proceso de convertir el ozono en oxígeno.
– Reemplazar aluminio por silicio en un tetraedro aumenta la carga negativa neta:
tetraedro fórmula estado de oxidación oxígeno estado de oxidación metal/semimetal carga en un tetraedro
SiO4 -2 +4 (Si) +4 + (4 x -2) = 4-
AlO4 -2 +3 (Al) +3 + (4 x -2) = 5-
Se requieren cationes para equilibrar la carga negativa de la estructura de aluminosilicato.
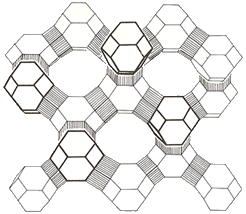
– Los tetraedros que contienen silicio y aluminio se disponen en marcos tridimensionales creando canales de interconexión y dando como resultado estructuras con una gran superficie.
Algunos de los usos de las zeolitas son:
- desecación
- reacciones de intercambio iónico
- catálisis de algunas reacciones
- separación de gases
DESECACIÓN
- La desecación se refiere a la eliminación del agua. Las zeolitas son desecantes o agentes secantes, pueden eliminar el agua de la atmósfera.
- La zeolita A es una zeolita sintética comúnmente utilizada en detergentes como suavizante de agua.
- La zeolita A tiene la fórmula Na12(Al12Si12O48)27H2O
- Na+ son los cationes que equilibran la carga en el ion aluminosilicato.
- La carga del ion aluminosilicato = 12 x +1 = 12+
- La fórmula del ion aluminosilicato es Al12Si12O4812+
- La zeolita también contiene 27 agua de cristalización (27H2O).
- El agua de cristalización retenida libremente se puede expulsar de la zeolita calentándola:
- Si se coloca la zeolita anhidra en aire húmedo, la zeolita absorberá el agua a medida que el sistema intenta restablecer el equilibrio según el principio de Le Chatelier.
INTERCAMBIO DE CATIONES
Dentro de los canales en la estructura de la zeolita, los iones, como el Na+, unidos iónicamente a la estructura de la zeolita, pueden ser desplazados por cationes de mayor carga.
El intercambio catiónico está determinado por:
- Fuerza de adsorción
- Concentraciones relativas de cationes en solución
![]()
ABLANDAMIENTO DEL AGUA
El agua dura que contiene Ca2+ o Mg2+ se puede pasar a través de una columna rellena con zeolita de sodio, NaZ.
Los cationes dipositivos Ca2+ o Mg2+ desplazan los iones Na+ de los canales dentro del marco de la zeolita:
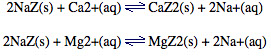
El Na+ no formará un precipitado con el jabón como lo hace el Ca2+ o el Mg2+, por lo que el agua se ha ablandado.
Dado que el intercambio catiónico es una reacción de equilibrio, es posible regenerar la zeolita de sodio pasando una solución concentrada de cloruro de sodio, o salmuera, a través de la zeolita.
El aumento de la concentración de Na+(aq) desplaza la posición de equilibrio hacia la izquierda por el Principio de Le Chatelier, favoreciendo la reformación de la zeolita sódica y liberando Ca2+ o Mg2+ de vuelta a la solución.
FERTILIZANTES NITROGENADOS DE LIBERACIÓN CONTROLADA
La urea es un fertilizante nitrogenado común, soluble en agua, que se puede filtrar a través de la zona de la raíz.
La urea se convierte en amoníaco por una enzima, la ureasa, que se encuentra en muchos suelos.
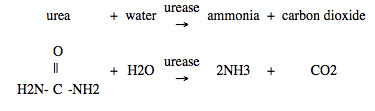
El amoníaco reacciona con el agua en el suelo para formar iones de amonio:
![]()
Las bacterias del suelo convierten los iones de amonio en iones de nitrato que se filtran fácilmente del suelo.
Las zeolitas se pueden utilizar para reducir la pérdida de este nutriente nitrogenado de tres formas:
- La urea puede estar contenida dentro de la estructura de zeolita, lo que evita que se filtre a la zona de la raíz.
- La urea contenida en la estructura de zeolita ralentiza la conversión de urea en iones de amonio por parte de las bacterias del suelo.
- La adsorción de iones de amonio en los canales de la zeolita los protege de las bacterias nitrificantes que los convierten en iones de nitrato lixiviables.
Los iones de amonio se liberan en el suelo lentamente con el tiempo.
FERTILIZANTES NITROGENADOS DE LIBERACIÓN CONTROLADA
Una zeolita que contiene un ion de intercambio como el amonio se puede mezclar con minerales de fosfato (como apatita, fosfato de calcio) para producir un fertilizante de fósforo de liberación controlada.
La zeolita toma Ca2+ de la apatita y libera iones de fosfato y amonio en el suelo:
![]()
A medida que las plantas absorben el fosfato, la zeolita liberará más iones de fosfato y amonio en un intento de restablecer el equilibrio según el principio de Le Chatelier.
CATÁLISIS
Los iones de hidrógeno, H+, se pueden incorporar a la estructura de la zeolita para lograr una compensación de carga.
Estos iones de hidrógeno se unen a los oxígenos puente dando como resultado grupos ácidos.
Estas zeolitas se comportan como ácidos y pueden iniciar una variedad de reacciones químicas dentro de sus canales.
Solo ciertas formas de moléculas podrán entrar y salir de los canales en la zeolita, por lo que se dice que el catalizador de zeolita es selectivo de forma.
Una zeolita particular se utiliza en la industria petroquímica como “catalizador de craqueo”.
Las moléculas de hidrocarburo de cadena larga que están presentes en los aceites pesados pueden difundirse a través de los canales de la estructura de la zeolita y hacia grandes cavidades donde son atacadas por los grupos ácidos de la zeolita y se descomponen (descomponen) en moléculas de hidrocarburo de cadena más corta.
SEPARACIÓN DE GASES
Las zeolitas se pueden utilizar para separar mezclas de diferentes gases.
Las moléculas gaseosas de la forma correcta pueden pasar (difundirse) a través de los canales de la zeolita.
Las moléculas gaseosas que no tienen la forma correcta no pueden pasar (difundirse).
Las moléculas de diferentes formas serán absorbidas y difundidas a través de la estructura de la zeolita en diferentes grados.
Los sistemas de generación de oxígeno a bordo se utilizan en aeronaves que vuelan a gran altura. Utilizan zeolitas para eliminar el nitrógeno del aire comprimido con el fin de suministrar oxígeno a las tripulaciones.
Esto se debe a que el N2(g) se adsorbe más fuertemente que el O2(g) en las zeolitas con una proporción baja de silicio a aluminio.
NANO
ATLAS
TITAN
MAGNUM