Introducción al Ozono
Esta es una introducción al ozono donde podrás conocer sus propiedades fundamentales.
¿QUÉ ES EL OZONO?
El ozono es una de las moléculas más abundantes en la atmósfera terrestre. El ozono es una molécula que consta de tres átomos de oxígeno cargados negativamente. La molécula de ozono es muy inestable y tiene una vida media corta, lo que hace que vuelva a su forma original después de un tiempo, de acuerdo con el siguiente mecanismo de reacción:
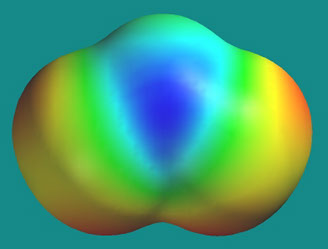
Principalmente, una molécula de ozono no es más que una molécula de oxígeno que ha recibido un átomo de oxígeno extra por alto voltaje eléctrico. El ozono se produce naturalmente a través de ciertos tipos de reacciones químicas. Un ejemplo bien conocido es la capa de ozono, que es creada por los rayos UV emitidos por el sol. El ozono también se forma durante las tormentas eléctricas, en las cascadas y, aunque se trata de un proceso menos natural, en el smog fotoquímico que se forma en verano. En las tormentas eléctricas, el ozono se forma como resultado de los altos voltajes involucrados. El característico olor fresco después de una tormenta eléctrica es causado por la formación de ozono.
Cuando se habla de ozono, los ejemplos antes mencionados se asocian inmediatamente con él. Sin embargo, es menos conocido que el ozono se puede producir artificialmente para que se pueda utilizar para el tratamiento del agua. Los generadores de ozono pueden crear ozono artificialmente por medio de voltajes extremadamente altos o por medio de luz ultravioleta. Ambos métodos implican la descomposición de la molécula de oxígeno. Esto provoca la formación de radicales de oxígeno. Estos radicales de oxígeno pueden unirse a las moléculas de oxígeno y formar ozono (O3).
OZONO UN OXIDANTE QUE QUEMA COMPUESTOS QUÍMICOS
El ozono es uno de los oxidantes más fuertes conocidos. El radical de oxígeno adicional en una molécula de ozono se une rápidamente a cada componente que entra en contacto. Esto se debe a la inestabilidad del ozono y su tendencia a volver a su forma original (O2). El ozono puede oxidar tanto sustancias orgánicas como inorgánicas (oxidación), pero también microorganismos como virus, bacterias y hongos (desinfección). Esto hace que el radical de oxígeno adicional se libere de la molécula de ozono y se una a otros materiales para que solo queden moléculas de oxígeno (O2) puras y estables.
Como resultado de los mecanismos de reacción mencionados anteriormente, el ozono se puede utilizar para una gran variedad de propósitos. El ozono se aplica principalmente en la purificación de aguas residuales y agua potable (para desinfección). La aplicación del ozono en la rama industrial es cada vez mayor. Por ejemplo, la industria alimentaria utiliza ozono para la desinfección y la industria textil utiliza ozono para la eliminación del color.
El mayor beneficio del ozono es su característica pura. Solo oxida sustancias y, como resultado, rara vez se produce la formación de subproductos.
NANO
ATLAS
TITAN
MAGNUM